|
|
上篇文章写了荧光蛋白的结构,但是鱼友最关心的问题无非是如何让珊 瑚产生更多的荧光蛋白以达到“发色”的效果。还是把最重要的理念性的话说在前头。想明白发色的问题一定要清楚的最重要的一点是:珊 瑚无论调高还是调低荧光蛋白的表达或者宽泛一点说生物的很多基因或者蛋白的的表达调控本质上都是一种对于环境变化的主动的适应性调控。
那么怎么样的环境才需要珊 瑚表达荧光蛋白去适应呢,很简单,想想荧光蛋白目前已知的主要功能是什么。对,很容易想到荧光蛋白的表达是对光环境的适应结果。事实上目前大部分研究都是支持这样的说法的。所以说如果一定要找一个影响荧光蛋白的决定性因素的话,一定是光不会有错了。
当然一定要注意的一点是,某种基因或者蛋白的出现并不是一种生物为了某个目的主动产生的,而是偶然间产生后可以提高生物对环境的适应能力经过自然选择被动的筛选留下来的,所以很多基因或者说蛋白本身可能就发挥了很多不同的功能,并不一定是因为某个单一的特定的目的留下来的,而且这些基因或者蛋白在经过些许的变化以后又有可能发挥其他的功能。
说回荧光蛋白,根据目前的假说和实验结果,很有可能需要把荧光蛋白分成两个维度来考虑。一类是绿色荧光蛋白和大部分色蛋白,这类蛋白可能更多的是发挥的光保护作用,这可能是因为绿色荧光蛋白普遍对荧光的转化效率高,也就是能把比较多的光能转化成荧光反射走,所以有比较好的光保护作用。
1、荧光蛋白的光保护作用
(1)比如Or等[1]把丛生盔形珊 瑚放置在不同水深下(众所周知水越深光强越弱),结果表明水深越浅绿色荧光的强度越强。但是就像我之前说的看文献是很有门槛的事情,绝不可以看了一篇文献就觉得知道了真相,比如Mazel等[2]之前的研究就表明绿色荧光的强度跟深度没有明显相关性。所以要更全面的阅读文献以后才能倾向于判断Mazel的研究更可能是特例或者是实验方法的原因。
Or等的这篇文章还发现不同的荧光蛋白分布的位置不同,有些在外胚层(虫黄藻在内胚层),更可能发挥了发挥了光保护的作用,有些在内胚层,有可能是发挥其他的作用比如接下来会讲的生产力假说。
(2)不要着急我们继续看,Cathyrn等[3]用同一种珊 瑚刺柄珊 瑚(Hydnophora grandis)(就是绿八仙)的高绿色荧光个体和低绿色荧光个体在高中低三种光强下做了实验,结果就很有意思了,在高光强下,高绿色荧光的个体的Fv/Fm值显著的高于低的,这个值你可以理解为虫黄藻的健康状况,也就是说绿色荧光蛋白较好的保护了珊 瑚和虫黄藻,而且生长速度也显著的高于低的个体,而在中光强下,二者的生长速率是差不多的,低光强下就更有意思了,反过来了,低荧光个体生长速度显著快于高荧光个体,高荧光个体几乎没长。
这可能是因为一方面表达更多的荧光蛋白消耗了更多的生长需要的资源,另一方面绿色荧光把更多的光反射走了虫黄藻可以用来光合作用的光更少了所以长的很慢。这里其实也可以看出基因的调控都是一种trade off,调高这一个基因在一方面获得优势在另一方面就会有劣势,比如一般提高了抗胁迫的能力可能生长能力就会更弱一些,在没有胁迫的环境下高抗胁迫的个体可能就竞争不过那些低抗胁迫的个体。
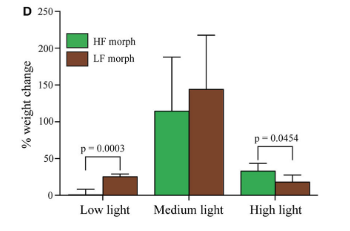
绿色的是高荧光个体,褐色的是低荧光个体,纵轴是生长速度
当然这种光保护效果在二十多年前就已经有报道了[4]。
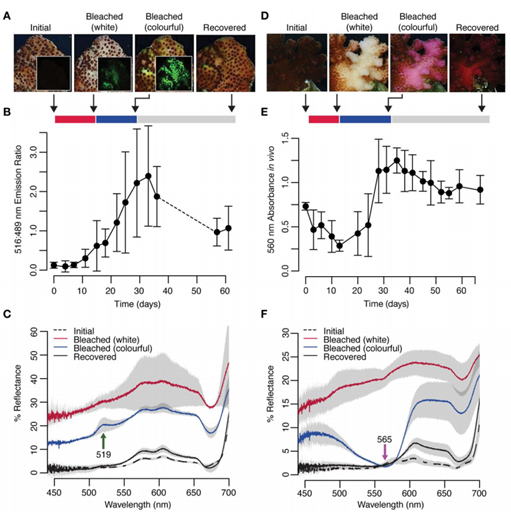
(3)还有一篇最近发在cell子刊current biology上的研究我觉得非常有意思[5],这篇我会写的比较仔细。作者注意到了一种情况,就是所谓的彩色白化(colorful bleaching),就是在比较中度的大面积白化现象里,这种情况下虫黄藻没了但是珊 瑚还相对健康,有能力进行一些调控,很多时候能恢复。出现这种白化后珊 瑚经常会出现非常妖艳的色彩,嗯就是鱼友最爱的糖果色。

这些珊 瑚并不是一开始就这么鲜艳的,而是出现了白化现象以后两到三周才开始变得更鲜艳的,这是为什么。作者分析了一个可能的原因,我们知道白色的东西就是因为可以反射所有波长的光线,珊 瑚的骨骼就是白色的,珊 瑚的组织又几乎是透明的,当没有了虫黄藻以后,射入到珊 瑚组织的光线被骨骼一反射又重新照到珊 瑚的组织上,所以珊 瑚组织受到的光照强了很多。
文章中的数据显示是反射率从百分之几提高到了30-40%左右,这就大大加剧了光对组织的损伤。文中进行了很多实验,可以说是非常严谨了(文中数据量非常大,我只选择性的贴了一些图表)。
首先用强红光诱导一种滨珊 瑚白化,白化后用强蓝光照射,一般倾向于在高光强下表达的绿色荧光蛋白表达量就不断增加,而一般倾向于在弱光下表达的青色荧光蛋白表达量却没有变化。那是不是白化了就会提高荧光蛋白表达呢,不是的,作者同时在白化后用同样光强的绿光照射珊 瑚,绿色荧光蛋白的表达就并没有增加。
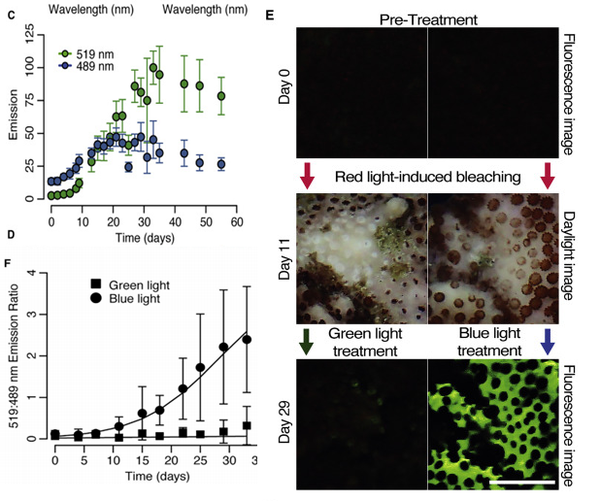
而如果直接用高温诱导白化模拟野外的情况,在高温白化大约三周后观察到了绿色荧光蛋白的大量表达,与野外2.5-3.5周的情况非常类似。
再换用其他的白化方式,使用高营养盐(嗯,高营养盐也是可以诱导白化的,这里准确的说是高硝酸盐)诱导白化后,蓝光下也出现了相同的情况,绿色荧光蛋白增加而青色荧光蛋白没有明显变化。
而绿色荧光蛋白换成了色蛋白以后的情况也是很类似的,作者用鹿角杯形珊 瑚(就是猫骨)在营养盐诱导白化以后,蓝光照射下粉色色蛋白显著增加而使用绿光照射就并没有明显变化。
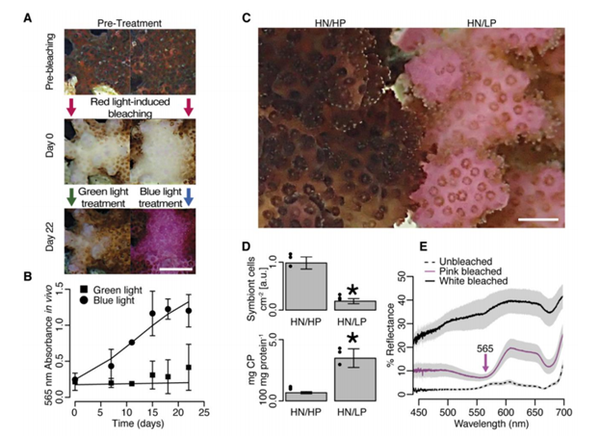
同样的对比有粉色色蛋白和没有粉色色蛋白的珊 瑚个体,有粉色色蛋白的个体虫黄藻的恢复更好。
使用另一种蔷薇珊 瑚(就是瓦)在营养盐诱导白化以后蓝光照射下也出现了很高水平的紫红色色蛋白的表达。
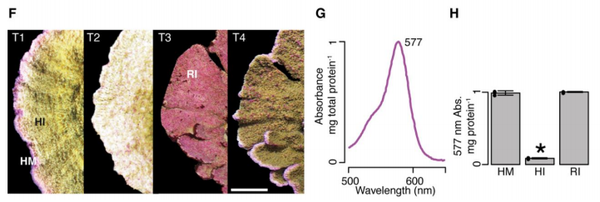
而且随着时间的推移,在虫黄藻慢慢恢复以后紫红色色蛋白的表达也重新恢复之前的水平。别的珊 瑚的绿色荧光蛋白也是类似的情况,在虫黄藻恢复后表达重新下降。
作者还提到了很有趣的一点,就是珊 瑚边缘的生长线的部分,这个部分是没什么虫黄藻的,这个部分就一直保持了很高的紫红色色蛋白的表达,这与我们经常见到的头顶的生长点是蓝色、紫色的是一致的,更加说明这些蓝色紫色的生长点是为了保护珊 瑚不受强光的损伤。从这个实验也可以看得出来荧光蛋白、色蛋白的高表达在环境胁迫解除以后是会重新下降而不是一成不变的,所以如何维持住荧光蛋白的表达确实是很需要水平的事情。
所以很多研究都表明往往高光强下珊 瑚倾向于表达绿色荧光蛋白和色蛋白,很多时候有鱼友说自己的缸里珊 瑚都绿了基本上跟所谓的铁多了没什么关系,最有可能是光强比较高造成的。当然也不一定是绿色荧光,像多孔鹿角珊 瑚(就是鱼鳞)常见的红色荧光本身荧光效率也非常高,不弱于绿色荧光蛋白,所以也有很好光保护功能[6],所以一般来说红鱼鳞怎么晒都不容易变绿色的。
2、荧光蛋白的生产力假说
其他颜色的荧光蛋白,尤其是LPS中常见的那些红色之类的荧光更有可能发挥的是另外一个作用,就是生产力假说。生产力假说认为在水深较深的环境里,珊 瑚需要把波长较短的蓝紫光转化成其他的波长更有利于光合作用。
(1)比如D'Anglo等[7]的研究就表明他们研究中的几种珊 瑚,体内的绿色、红色荧光蛋白和色蛋白在低光强下几乎就不表达,而在高光强下光强越强表达越高,相反的青色荧光蛋白在低光强下就有很高的表达。
要注意的是荧光蛋白并不是简单的按照颜色来分类的,同样是红色荧光蛋白,鱼鳞中的红色荧光蛋白就和富士脑中的红色荧光蛋白的光学特性完全不一样,发挥的功能也很可能完全不同。
(2)Edward等[8]的研究就用两种LPS,一种脑和调色盘,分别找来有红色荧光的个体和没有红色荧光的褐色个体,在较低的蓝光下饲养,有红色荧光的个体存活率明显高于没有的个体,到最后褐色个体几乎全部死亡,而使用同样强度的白光饲养,有红色荧光的个体依然活的很好,褐色个体虽然也死亡了一部分,但是依然有一定成成活率。而且从野外调查来看,水深越深的区域红色个体的占比也越高
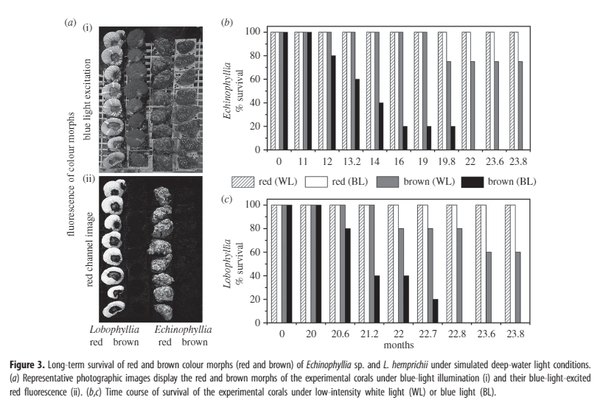
(3)Gal等[9]的研究也表明了类似的结果,他们研究中的几种珊 瑚深水区的个体里黄色橘红色的个体显著多余浅水区。要注意的是从上面的研究也可以看出很多珊 瑚可能缺乏大幅度改变荧光蛋白表达的能力,所以可能只能适应某些范围的光照,而无法通过光照改变调节其颜色。
有些鱼友可能会说为什么跟我感觉的不一样,其实很重要的原因是好的科学实验是在严格的控制变量的情况下进行的,但是鱼友缸里的珊 瑚种类各种各样,甚至连实验重复都没有,来自各个不同的海域,不同的国家,野外适应的环境也完全不同,再加上荧光蛋白本身现在科学家就认识到可能发挥了很多不同的作用,所以在某一个特定的环境下产生各种完全不同的响应甚至找不到一丝规律都是很正常的事情。
最近还看到有人发Dana Riddle在18年MACNA演讲的时候贴的一张图
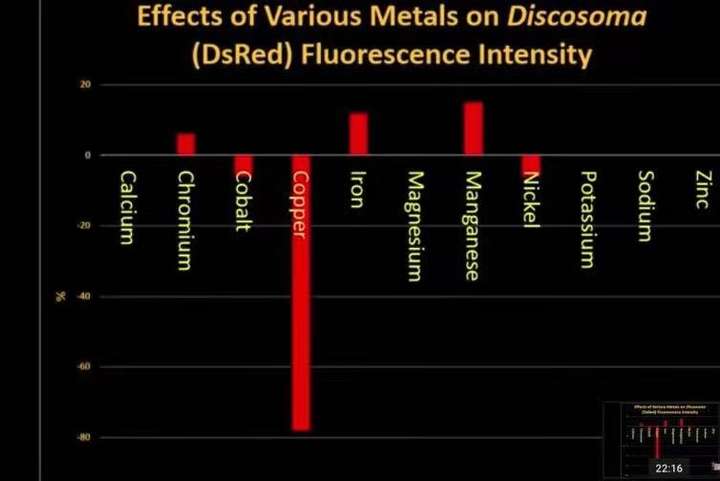
其实这个图反而是更说明金属离子的添加对荧光蛋白没什么影响的。升高的那两个镁和铁差别也就百分之十几出头,非常业余的没有标error bar,这点差别基本上只要标准差不是特别小统计检验上大概率都是检验不出差别的,所以其实结论就是这些离子对荧光蛋白的荧光效率没什么太大影响。退一万步说,就算有这么点百分之十的差别你肉眼是根本无法察觉的,人眼对光线的感知压根就不是线性的,而是对数的,你随便往缸里看一眼灯正下方跟往旁边挪个十厘米光强差都比这大,你看你看得出区别么。再说退一万步说,就算是有影响而且你看得出来,人家做的这个是红色荧光蛋白,铁离子提高红色荧光蛋白也跟那些狗屁倒灶的理论里铁提升绿色对不上啊,这算蒙都没蒙中好么。 唯一一个真正能看出肯定有显著影响的是什么,就是那个柱子最长的铜离子,为什么铜有这么大影响,原因也非常简单,学过有机化学的人都能明白,其实就是重金属离子导致了蛋白质的变性,引起了荧光淬灭而已。
最后我觉得最重要的一点是,从上面的很多实验也可以看出,决定珊 瑚荧光蛋白表达的决定性因素是光,但是光绝对不是影响荧光蛋白的唯一因素,而是与其他的环境因子共同相互作用下产生影响,所以改变其他的环境因子依然是可以改变荧光蛋白的表达的。当然这几年越来越多的鱼友可以养出神奇的色彩我觉得主要是两个原因,一个是因为随着产业的发展越来越多本身就非常漂亮的个体出现在市场上,一个是因为LED的普及,有经验的厂商可以精准的做出有利于荧光蛋白的光谱,像以前的金卤和T5是基本不可能实现的。从思路上来讲,用严格控制营养盐等一些手段限制虫黄藻的增多(当然这点在挑珊 瑚的时候实际上就开始了,有些个体本来就倾向于较少的虫黄藻,也有个体倾向于表达更多、更多种类的荧光蛋白,归根到底其实就是--挑贵的一般是没错的),保持珊 瑚健康(不然珊 瑚也没有力气给你分泌荧光蛋白),这要通过合理的光照环境和喂食(不一定是直接喂食珊 瑚,通过喂鱼也是一种很好的手段)还有很好的水质,最后再有高质量的LED光源(选公认的基本上就可以了)就完全可以实现。当然说起来容易做起来还是没那么容易的。
参考文献:
[1] Ben-Zvi O , Eyal G , Loya Y . Light-dependent fluorescence in the coral Galaxea fascicularis[J]. Hydrobiologia, 2014, 759(1):1-12.
[2] Mazel C H , Lesser M P , Gorbunov M Y , et al. Part 2; Light in Shallow Waters || Green-Fluorescent Proteins in Caribbean Corals[J]. Limnology & Oceanography, 2003, 48(1):402-411.
[3] Cathryn Q , Cecilia D , J?Rg W . Trade-Offs Associated with Photoprotective Green Fluorescent Protein Expression as Potential Drivers of Balancing Selection for Color Polymorphism in Reef Corals[J]. Frontiers in Marine Science, 2018, 5:11-.
[4] Salih A , Larkum A , Cox G , et al. Fluorescent pigments in corals are photoprotective[J]. Nature, 2000, 408(6814):850-3.
[5] Bollati E , D'Angelo C , Alderdice R , et al. Optical Feedback Loop Involving Dinoflagellate Symbiont and Scleractinian Host Drives Colorful Coral Bleaching[J]. Current Biology, 2020, 30(13).
[6] Gittins J R , D'Angelo C , Oswald F , et al. Fluorescent protein‐mediated colour polymorphism in reef corals: multicopy genes extend the adaptation/acclimatization potential to variable light environments[J]. Molecular Ecology, 2014, 24(2):453-465.
[7] D'Angelo C , Denzel A , Vogt A , et al. Blue light regulation of host pigment in reef-building corals[J]. Marine Ecology Progress, 2008, 364(jul.29):97-106.
[8] Edward, G, Smit, et al. Acclimatization of symbiotic corals to mesophotic light environments through wavelength transformation by fluorescent protein pigments[J]. Proceedings of the Royal Society B Biological Sciences, 2017.
[9] Gal E , J, Rg W , Mila G , et al. Spectral Diversity and Regulation of Coral Fluorescence in a Mesophotic Reef Habitat in the Red Sea[J]. Plos One, 2015, 10(6):e0128697.
|
|
 |Archiver|手机版|小黑屋|海友网CMF
( 琼ICP备12003277号 )
|Archiver|手机版|小黑屋|海友网CMF
( 琼ICP备12003277号 )